岳伟华课题组针对抑郁焦虑障碍联合提出基于CYP2D6活性评分的帕罗西汀精准给药新策略
2024年5月21日,北京大学第六医院、IDG麦戈文脑科学研究所岳伟华教授课题组,与武汉大学人民医院刘忠纯教授、河北省精神卫生中心张云淑教授和重庆医科大学附属第一医院况利教授团队联合全国17家分中心,在柳叶刀子刊 eBioMedicine 发表题为“Dose adjustment of paroxetine based on CYP2D6 activity score inferred metabolizer status in Chinese Han patients with depressive or anxiety disorders: a prospective study and cross-ethnic meta-analysis”的研究论文。
本研究通过前瞻性队列研究和跨种族meta分析,首次在中国汉族抑郁障碍和焦虑障碍患者中探讨了基于CYP2D6活性评分的帕罗西汀精准给药策略。研究发现,基于CYP2D6活性评分推断的CYP2D6酶的代谢状态显著影响了帕罗西汀的稳态血药浓度、疗效和不良反应,且性别和种族也是重要的影响因素,为帕罗西汀的精准用药提供了重要的科学依据,有助于改善中国汉族抑郁障碍和焦虑障碍患者的治疗效果和安全性。本研究是抑郁和焦虑障碍改善精准医学联盟(Precision Medicine to Enhance Depression and Anxiety Outcome, PMEDA)的重要研究成果。

抑郁障碍和焦虑障碍在全球范围内是导致残疾和疾病负担增加的主要精神疾病,严重影响患者的日常生活和社会功能,极大地降低了患者的生活质量。尽管在临床实践中,帕罗西汀等抗抑郁药物已经被广泛使用,但患者对这些药物的反应存在显著的个体差异。CYP2D6酶是细胞色素P450酶家族中的一个重要成员,负责代谢帕罗西汀在内的多种药物。某些个体由于携带CYP2D6基因的遗传变异,表现为CYP2D6快速代谢型或慢代谢型,这可能导致药物在体内的浓度不足或过高,从而影响治疗效果或增加发生不良反应的风险。因此,深入研究CYP2D6基因多态性与帕罗西汀疗效及安全性之间的关系,对于实现精准医疗、提高治疗效果和减少不良反应具有重要意义。
以下为主要研究结果:
本研究为一项为期8周的多中心、帕罗西汀单药治疗的前瞻性队列研究(PMEDA 研究),共纳入921名重性抑郁障碍、广泛性焦虑障碍和惊恐障碍的患者。根据CYP2D6基因分型结果计算CYP2D6活性评分,并据此将患者分为四种CYP2D6代谢型:慢代谢型(PMs)、中间代谢型(IMs)、广泛代谢型(EMs)和超快代谢型(UMs)。

图1 PMEDA研究概念图
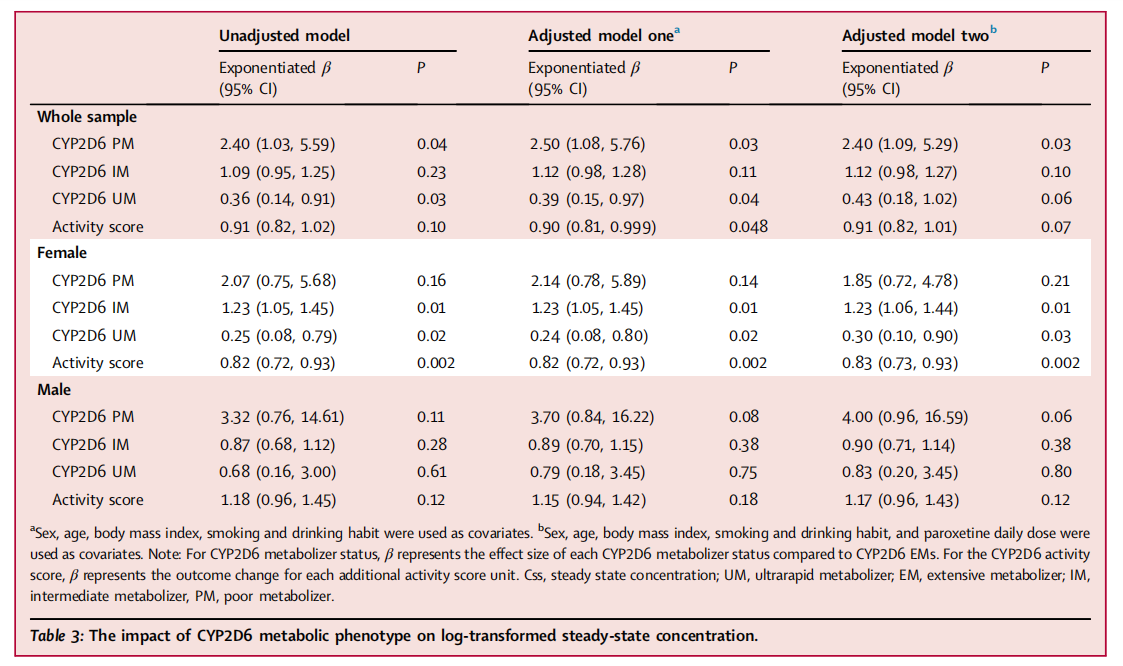
通过多重线性回归分析,结果显示在控制了年龄、性别、BMI、吸烟和饮酒习惯等预定义的混杂因素后,CYP2D6代谢表型(包括活性评分和代谢型)与帕罗西汀的稳态血药浓度显著相关。具体来说,PMs、IMs和UMs的帕罗西汀稳态浓度分别为EMs的2.50、1.12和0.39倍。其中PM/UM和EM的差异具有统计学意义(多元线性回归,指数化β = 2.50, 95% CI: 1.08 - 5.76, P = 0.03; 指数化β = 0.39, 95% CI: 0.15 - 0.97, P = 0.04)。进一步的亚组分析显示,女性患者IM/UM和EM的帕罗西汀稳态浓度差异具有统计学意义,但男性患者中的比较未发现显著差异。类似的,CYP2D6活性评分与帕罗西汀稳态浓度的关联在女性患者中具有统计学意义。
表 CYP2D6代谢表型与帕罗西汀对数转换稳态浓度的关联
本研究进一步发现,在重性抑郁障碍患者中,与EM者相比,UM者在帕罗西汀治疗4周后具有更差的治疗效果。具体而言,在控制年龄性别的协变量后,效应具有一定的趋势 (标准化β = −0.93, SE = 0.50, P = 0.07); 进一步控制病程、基线严重程度、药物剂量和合并用药情况等协变量后,效应达到统计学显著(标准化β = −0.98, SE = 0.50, P = 0.049)。通过限制性立方样条(RCS)回归分析,研究进一步探索了CYP2D6活性评分与不良反应之间的非线性关系。图2a展示了CYP2D6活性评分与帕罗西汀不良反应的RCS曲线,揭示了在不同活性评分 (Activity Score, AS) 水平下不良反应发生风险的变化趋势。曲线表明,在AS的低值区域(即AS < 1.63,包括PMs、IMs和部分EMs),随着AS的降低,不良反应的发生风险增加;而在AS的高值区域(即AS ≥ 1.63,包括UMs和部分EMs),这种关系变得不明显。图2b则通过多重线性回归模型计算了在AS低于和高于1.63的亚组中,AS每增加一个标准差时发生不良反应的风险比(Odds Ratio, OR),在AS小于1.63的患者中,AS每减少一个单位,ADR的风险就增加127%(OR = 0.38, 95% CI: 0.20 - 0.74, P = 0.005)。
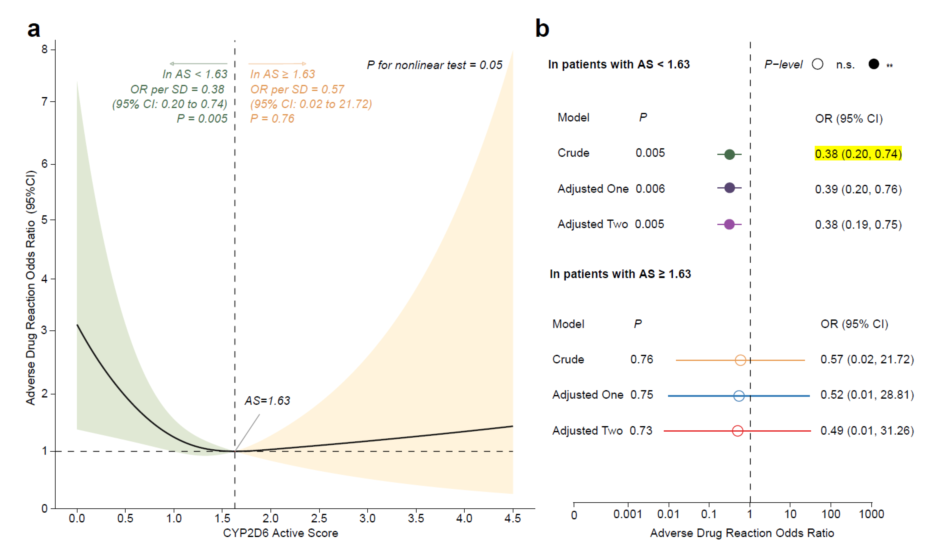
图2 CYP2D6活性评分与药物不良反应(ADR)发生风险的关联
为了进一步探究CYP2D6基因的拷贝数变异(CNV)如何影响帕罗西汀的药代动力学和疗效,研究团队采用基因分型技术来确定患者CYP2D6基因的拷贝数。结果显示,控制预先定义的混杂因素后,CYP2D6基因拷贝数缺失携带者的帕罗西汀稳态浓度为正常拷贝数携带者的1.53倍 (指数化β = 1.53, 95% CI: 1.26-1.85, P < 0.001)。此外,CYP2D6基因拷贝数缺失携带者在8周帕罗西汀治疗后的症状改善程度更大(汇总标准化β = 0.21, 95% CI: 0.01-0.41, P = 0.04, I2 < 0.01)。
此外,研究团队致力于在中国人群中,界定帕罗西汀治疗抑郁障碍和焦虑障碍的治疗参考范围(Therapeutic Reference Range, TRR),目的是让临床医生能够依据患者的血药浓度来调整剂量,以提高疗效和降低不良反应。通过受试者工作特征曲线(ROC)分析,研究确定了区分治疗应答者与非应答者或有/无不良反应的血药浓度最佳临界值(图3)。结果显示,对于抑郁障碍和焦虑障碍患者来说,帕罗西汀的TRR为31.95–79.65 ng/ml,在此浓度范围内的患者具有更高的治疗应答率(OR = 1.47, 95% CI: 1.11–1.95, P = 0.01) 和更低的不良反应发生率(OR = 0.44, 95% CI: 0.26 - 0.76, P = 0.003)。特别地,对于抑郁障碍患者,TRR被细化为31.55-52.5 ng/ml。与未处于TRR的患者相比,处于TRR的患者展现出更高的治疗应答率(OR = 1.74, 95% CI: 1.22-2.49, P = 0.002)和更低的不良反应发生率(OR = 0.38, 95% CI: 0.19-0.72, P = 0.004)。
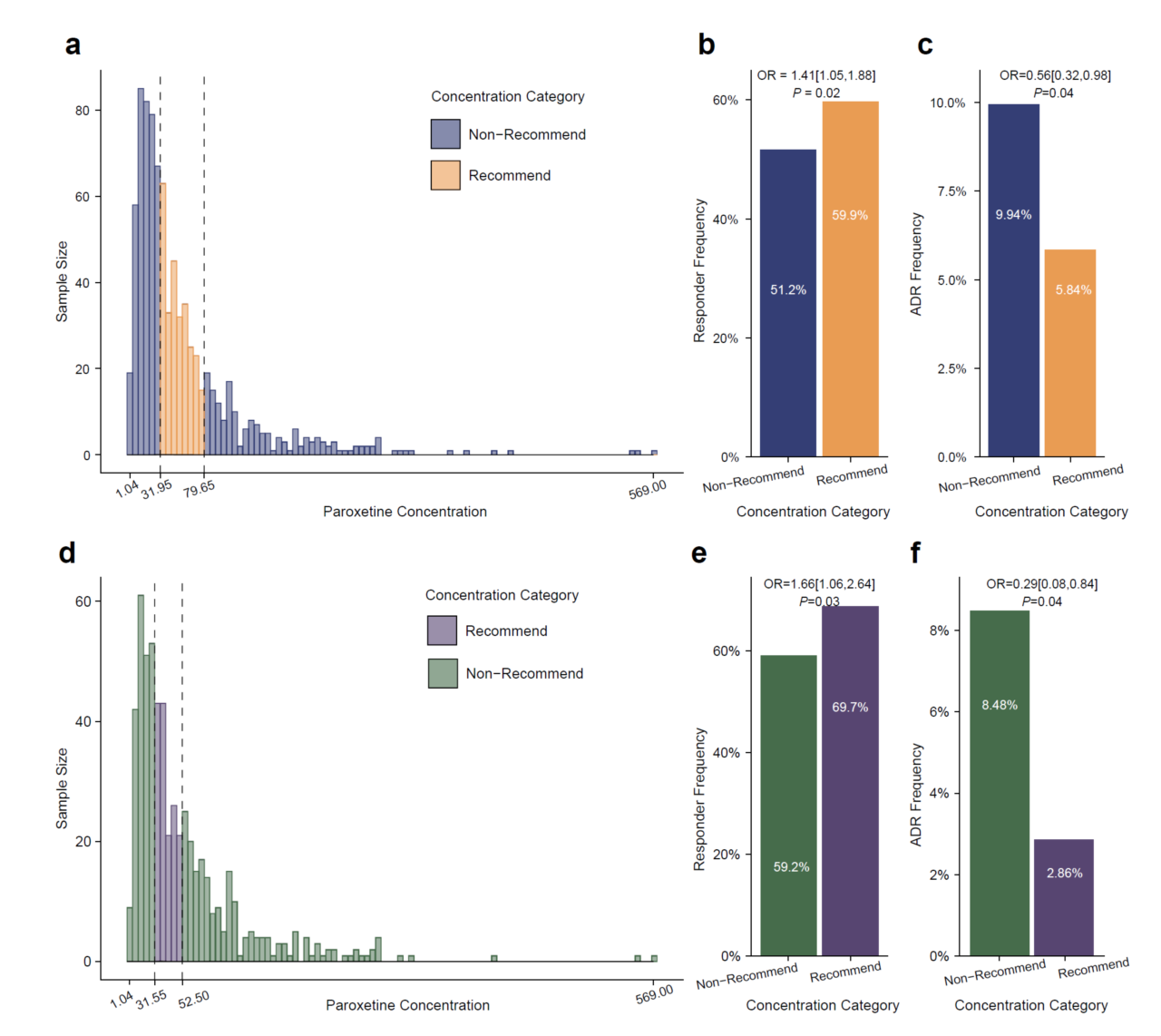
图3 中国汉族人群中抑郁和焦虑障碍患者的治疗参考范围。
随后,本研究根据不同CYP2D6代谢型的帕罗西汀药代动力学参数差异来计算剂量调整比例 (图4)。具体而言,针对女性患者PMs、IMs、EMs和UMs,计算得到的剂量调整比例分别为制造商推荐剂量的69%、98%、104%和479%;而对于男性患者则分别为40%、114%、94%和225% (图4a)。值得注意的是,研究指出,由于PMs和EMs的帕罗西汀稳态浓度差异的95% 置信区间相对较大,故在临床实践中应用此推荐调整比例仍需要谨慎,同时,对于男性患者IM/UM者,本研究暂不支持直接进行剂量调整,由于上述代谢型与EM的比较在男性亚组分析中并没有达到统计学显著。
此外,研究还借助跨种族meta分析结果,为东亚和非东亚人群提供了差异化的剂量调整建议(图4b)。这一分析考虑了种族间CYP2D6代谢型对帕罗西汀药代动力学参数的影响,并据此计算了相应的剂量调整比例。具体而言,东亚人群中PMs、IMs、EMs和UMs的剂量调整比例分别为制造商推荐剂量的35%、40%、143%和241%;非东亚人群则分别为62%、68%、131%和159% (图4b)。这些建议不仅为个体化药物治疗提供了科学依据,还为实现不同种族和性别背景患者的精准医疗提供了实践指导。
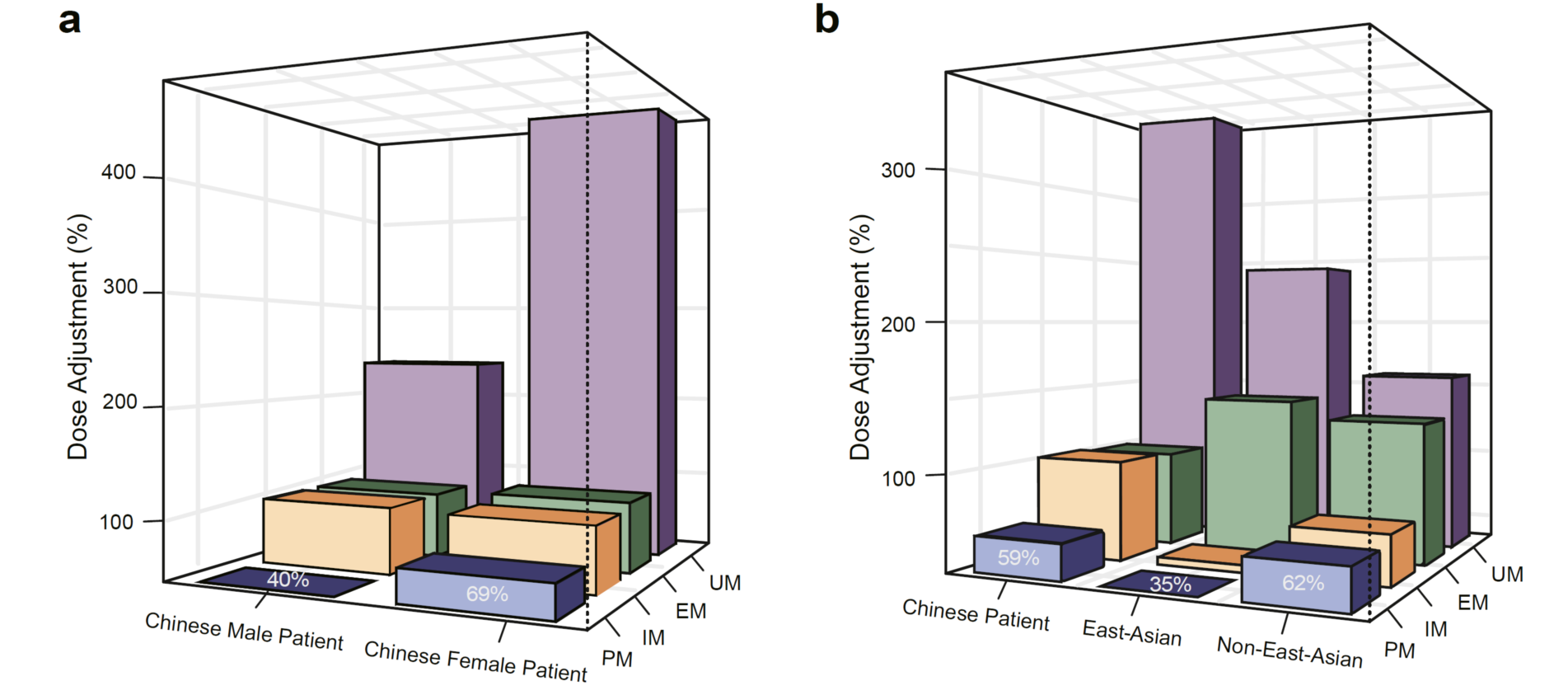
图4 基于不同CYP2D6代谢型的帕罗西汀剂量调整策略
综上所述,这项研究的发表为临床医生提供了基于CYP2D6代谢型进行帕罗西汀剂量调整的科学依据,有助于改善中国汉族患者的治疗效果和安全性。同时,研究结果有助于推动个性化药物治疗的发展,促进精准医疗在精神科领域的应用。本研究共同第一作者为北京大学第六医院博士生廖云丹和孙玉涛医生,最后通讯作者为北京大学第六医院岳伟华教授,武汉大学人民医院刘忠纯教授、河北省精神卫生中心张云淑教授和重庆医科大学附属第一医院况利教授为本研究的共同通讯作者。
全文链接
Liao, Y., Sun, Y., Guo, J., Kang, Z., Sun, Y., Zhang, Y., He, J., Huang, C., Sun, X., Zhang, J. M., Wang, J., Wang, H. N., Chen, Z. Y., Wang, K., Pan, J., Ni, A. H., Weng, S., Wang, A., Cao, C., Sun, L., … Precision Medicine to Enhance Depression and Anxiety Outcome Consortium (2024). Dose adjustment of paroxetine based on CYP2D6 activity score inferred metabolizer status in Chinese Han patients with depressive or anxiety disorders: a prospective study and cross-ethnic meta-analysis. EBioMedicine, 104, 105165.
https://doi.org/10.1016/j.ebiom.2024.105165